효소의 역가 단위
효소의 국제 단위(unit)
240 KNU-T/g = nnnn WGV =nnnn EGU(Endo Glucanase Units)
이거 환산이 가능한지?
몰라서 Study한 내용이다.
아직 답을 찾지 못한 상태임.
효소가 최적조건하, 30℃에서 1분 당 1μmol의 기질을 생성물로 변환시키는데 필요한 효소의 양을 1 단위(1 IU = 1μmol·min-1)라 한다. 또 신국제단위로서 katal(kat)도 이용되고 있으며 1 kat는 1초에 1mol의 기질을 변환하는 효소활성량을 말하며 1 kat = 6 x 107IU이다. 효소의 농도는 1㎖ 중의 효소를 단위수로 표시한다.
The enzyme unit (U) is a unit for the amount of a particular enzyme. One U is defined as the amount of the enzyme that catalyzes the conversion of micro mole of substrate per minute. The conditions also have to be specified: one usually takes a temperature of 25°C[2] and the pH value and substrate concentration that yield the maximal substrate conversion rate. The enzyme unit was adopted by the International Union of Biochemistry in 1964. Since the minute is not an SI unit, the enzyme unit is discouraged in favour of the katal, the unit recommended by the General Conference on Weights and Measures in 1978 and officially adopted in 1999. One katal is the amount of enzyme that converts 1 mole of substrate per second, so
- 1 U = 1/60 micro katal = 16.67 nano katal.
The enzyme unit should not be confused with the International Unit (IU), an unrelated measure of biologically active substances.
효소의 비활성(specific activity)
효소 1mg 당의 국제단위(IU)로 나타내며 신국제단위에서는 효소 1kg 당의 katal(kat)수로 나타낸다. 효소의 비활성은 효소제품의 순도를 나타내는 것으로 효소의 정제가 진행됨에 따라 비활성이 증가하고 최후에는 일정하게 된다.
효소의 분자활성(mol 활성; molecular activity)
1분간에 효소 1분자가 생성물로 변환하는 기질분자의 수를 말한다. 효소의 초기농도를 [E]0라 하면 효소의 최대반응속도 Vmax = κ[E]0로 되며 κ가 분자활성에 해당한다. 즉 κ = Vmax/[E]0로 된다. Carbonate dehydratase의 분자활성은 κ = 107분자/min으로 활성이 큰 효소라는 것을 나타내고 있다. 이전에는 대사회전수 또는 turnover number라 하였다.
촉매중심활성(활성중심 활성: catalytic center activity)
효소분자의 활성중심 1개당 1분간에 생성물로 변환시키는 기질분자의 수를 말하며 활성중심이 여러개인 경우에는 분자활성을 활성중심의 수로 나눈 값을 말한다.
효소의 반응특성
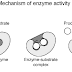
효소의 촉매작용은 효소가 존재하지 않는 상태에 비해서 그 반응의 활성화에너지(ΔE)를 저하시킨다. 효소의 촉매작용에 기여하는 것으로 생각되는 다음과 같은 몇 가지의 인자가 활성화에너지를 저하시키는 것으로 생각되고 있다.
① 기질의 접근과 유도 : 효소는 활성부위로 기질의 접근과 유도를 시도한다.
② 기질구조의 변화 : 효소의 유도적합으로 활성부위의 구조가 변화되면 결합한 기질의 구
조도 변화하게 된다.
③ 산 염기 촉매작용 : 효소의 활성부위는 아미노산 잔기의 치환기 R-로 되어 있으며 이들
의 일반적인 산, 염기부분은 수계(水界)에서 대부분 유기화학반응의 강력한 촉매작용을 일으킨다.
④ 공유결합 촉매작용 : 효소는 기질과 불안정한 효소-기질 공유결합 중간체를 형성한다.
효소의 제1단계의 분류는 다음과 같이 6군으로 분류된다.
① 제1군 산화환원효소(酸化還元酵素):이 군은 산화환원 반응에 관여하는 모든 효소들을 포함한다.
② 제2군 전이효소(轉移酵素):어떤 분자에서 기능기(機能基:화학반응에 동시에 관여하는 몇 개의 원자의 집단)를 떼어내어 다른 분자에 옮겨주는 효소들을 포함한다.
③ 제3군 가수분해효소(加水分解酵素):고분자(高分子:분자량이 큰 유기화합물 분자)를 가수분해하여 저분자(低分子)로 하는 효소들을 포함한다. 가수분해는 물분자를 첨가하여 큰 분자를 쪼개는 반응이다.
④ 제4군 리아제(lyase):기질로부터 가수분해에 의하지 않고 어떤 기(基:몇 개의 원자들의 집단)를 떼어내어 기질분자에 이중결합(二重結合)을 남기거나 또는 이중결합에 어떤 기를 붙여주는 효소들을 포함한다.
⑤ 제5군 이성질화효소(異性質化酵素):기질 분자의 분자식은 변화시키지 않고 다만 그 분자구조를 바꾸는 데에 관여하는 모든 효소들을 포함한다.
⑥ 제6군 리가아제(ligase):합성효소(合成酵素)라고도 부르는 것으로, ATP(아데노신삼인산)라는 물질 또는 이와 유사한 물질로부터 인산기(燐酸基)를 떼어내면서 그 때 방출되는 에너지를 이용하여 어떤 두 물질을 결부시키는 효소들을 총칭한다.
소화효소
소화효소는 그것이 분해하는 유기물의 종류에 따라 단백질 가수분해 효소, 탄수화물 가수분해 효소, 지방 가수분해 효소 등으로 분류된다.
⑴ 단백질 가수분해 효소:
단백질을 아미노산 또는 여러 가지 길이의 펩티드로 분해하는 효소이다. 단백질은 20종의 아미노산 분자가 수십 또는 수백 개의 펩티드결합을 통해 연결된 물질이다. 단백질 가수분해 효소는 이 펩티드결합을 끊어서 단백질 분자를 여러 도막으로 만든다. 사람의 경우, 소화효소 가운데 단백질 가수분해 효소로는 펩신 ·트립신 ·키모트립신 ·디펩티다아제 ·카르복시펩티다아제 ·아미노펩티다아제 등이 있다. 펩신은 위액 속에 들어 있는 효소인데, 위 속으로 분비될 때는 비활성형인 펩시노겐 형태로 분비된다. 그리고 위 속에서 염산의 작용을 받아 그 분자의 일부가 떨어져 나가면서 남은 부분이 활성형인 펩신이 된다. 이 효소는 단백질 분자에서 페닐알라닌 ·트립토판 ·글루탐산 등의 아미노산의 아미노기가 관여하고 있는 펩티드결합만을 끊는다. 따라서 단백질 분자는 곳곳에서 펩티드결합이 끊어져 여러 도막으로 잘린다. 이러한 도막들을 펩티드라고 한다. 펩신은 극도의 산성용액 속에서만 그 활성이 나타나므로 위 속에서만 단백질을 분해할 수 있다. 위 속은 위액과 함께 분비된 염산으로 말미암아 pH가 1~2 정도의 산성을 띠고 있다. 트립신과 키모트립신은 다같이 이자에서 만들어져 이자액과 함께 십이지장 속으로 분비되어 단백질을 가수분해한다. 트립신은 리신이나 아르기닌과 같은 아미노산의 카르복시기가 관여하고 있는 펩티드결합만을, 또 키모트립신은 페닐알라닌이나 티로신과 같은 아미노산의 카르복시기가 관여하고 있는 펩티드결합만을 선택적으로 가수분해하기 때문에, 이들의 작용을 받은 단백질은 역시 여러 가지 길이의 펩티드로 잘린다. 이 두 효소는 pH 7 근처인 중성에서 그 활성이 나타난다. 카르복시펩티다아제와 아미노펩티다아제는 모두 이자와 소장의 벽에서 분비되는데, 앞의 것은 단백질 분자의 카르복시기가 있는 말단에서, 그리고 뒤의 것은 그 반대쪽인 아미노기가 나와 있는 말단에서 펩티드결합을 차례차례로 끊기 때문에, 이들 효소의 작용으로 단백질에서부터 아미노산이 한 분자씩 유리되어 나온다.
⑵ 탄수화물 가수분해 효소:
아밀라아제 ·말타아제 ·락타아제 ·수크라아제 등의 탄수화물 가수분해 효소가 사람의 소화샘에서 분비된다. 사람이 섭취하는 탄수화물은 주로 녹말과 글리코겐인데, 이들은 모두 포도당 분자가 수백, 수천 개 길게 또는 가지를 치면서 연결되어 있는 고분자이다. 탄수화물 가수분해 효소는 이 녹말이나 글리코겐에 작용하는 효소인데, 아밀라아제는 이들을 엿당(말토오스)으로까지 분해한다. 말토오스는 2분자의 포도당이 연결된 물질이다. 아밀라아제는 침과 이자액 속에 들어 있다. 침 속의 아밀라아제는 프티알린이라고도 한다. 아밀라아제의 작용으로 생성된 말토오스는 이자와 소장에서 분비되는 말타아제에 의하여 2분자의 포도당으로 분해되고, 이 포도당이 소화관에서 모세혈관 속으로 흡수된다. 락타아제는 젖이나 우유 속에 많이 들어 있는 젖당[乳糖]을 그 구성성분인 포도당과 갈락토오스로 분해하는 효소로서 소장의 벽에서 분비된다. 수크라아제는 수크로오스[蔗糖]를 포도당과 과당(프룩토오스)으로 분해하여 각각 흡수되도록 하는 효소인데, 소장의 벽에서 장액과 함께 분비된다.
⑶ 지방 가수분해 효소:
리파아제가 있다. 음식물 속의 지방은 대부분이 중성지방이라고 하는 물질인데,
이것은 지방산 3분자가 글리세롤 1분자와 결합하고 있는 물질이다. 리파아제는 이 중성지방에 작용하여 지방산과 글리세롤로 분해하는 효소로서 이자에서 만들어져 십이지장에서 분비된다. 중성지방을 구성하는 지방산에는 여러 가지가 있으므로 중성지방의 종류도 매우 많다. 이 중성지방은 물에 잘 녹지 않기 때문에 소화관 속에서도 리파아제의 작용을 잘 받지 않는다. 그러나 쓸개즙 속의 각종 유기산염이 이 중성지방을 물에 녹는 형태로 바꾸어줌으로써 리파아제의 가수분해 작용이 비로소 나타나게 된다. 사람의 소화관에서는 이 밖에도 DNA(디옥시리보핵산) 가수분해 효소, RNA(리보핵산) 가수분해 효소 등도 포함되어 있으나, 음식물 속에 들어 있는 DNA나 RNA의 양은 극히 적기 때문에 이들 효소의 작용은 그다지 현저하지 않다.















0 개의 댓글: